您现在的位置是: 首页 > 分数线 分数线
高考化学同分异构体,高考化学同分异构体题目
tamoadmin 2024-06-28 人已围观
简介1.(高考)+化学:1,同位素.2,核素3,同素异形体4,同分异构体这四个的含义2.如何辨别有几种同分异构体3.分子式为C4H8Cl2的同分异构体有多少种 麻烦画一下结构简式 高中化学它分为构造异构和立体异构2类。 而立体异构又分为顺反异构(Z)(E)、光学异构、对映异构、构象异构等。 CH3 ⒈结构异构:结构不同引起异构 | (1)同系的异构化学性质相似,物理性质不同,如:正丁烷(CH3(CH2
1.(高考)+化学:1,同位素.2,核素3,同素异形体4,同分异构体这四个的含义
2.如何辨别有几种同分异构体
3.分子式为C4H8Cl2的同分异构体有多少种 麻烦画一下结构简式 高中化学
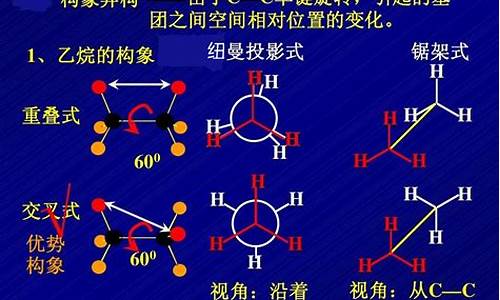
它分为构造异构和立体异构2类。 而立体异构又分为顺反异构(Z)(E)、光学异构、对映异构、构象异构等。 CH3 ⒈结构异构:结构不同引起异构 | (1)同系的异构化学性质相似,物理性质不同,如:正丁烷(CH3(CH2)2CH3)和异丁烷(CH3CHCH3) (2)不同系的同分异构体化学性质和物理性质都不同,如:乙醇(CH3CH2OH)和甲醚(CH3-O-CH3) ⒉立体异构:结构相似,但由于微小偏差导致结构不同 ①顺反异构:立体异构的一种,由于双键不能自由旋转引起的,一般指烯烃的双键,也有C=N双键,N=N双键及环状等化合物的顺反异构。 顺式异构体:两个相同原子或基团在双键同一侧的为顺式异构体,也用 cis- 来表示。 反式异构体:两个相同原子或基团分别在双键两侧的为反式异构体,也用 trans- 来表示。 顺反异构体产生的条件:⑴ 分子不能自由旋转(否则将变成另外一种分子);⑵ 双键上同一碳上不能有相同的基团; a d a a ╲ ╱ ╲ ╱ C ══ C & C ══ C ╱ ╲ ╱ ╲ b a b d ②旋光异构(对映异构):互为物体与镜像关系的立体异构体,称为对映异构体 (简称为对映体). 对映异构体都有旋光性,其中一个是左旋的,一个是右旋的. 所以对映异构体又称为旋光异构体. ③光学异构: 构造相同的分子,如使其一平面偏振光向右偏转,另一侧向左。则两种互为光学异构体。(.所谓光学异构体指分子结构完全相同,物理化学性质相近,但旋光性不同的物质) ④.构象异构:同一种化合物的构象,可通过单键旋转由一种变为另一种,则这两种互为构象异构体。 [高考考点]同分异构特点: 1.分子式相同,相对分子质量相同。 2.同分异构体的最简式相同,但最简式相同的不一定是同分异构。 3.结构不同。同分异构可以是同一类物质,也可以不是。
(高考)+化学:1,同位素.2,核素3,同素异形体4,同分异构体这四个的含义
同分异构体种类数目迅速看出来的方法:
(1)记忆法:
1、甲烷,乙烷,丁烷无同分异构体;
2、丁烷,丁炔,丙基,丙醇有两种同分异构体(仅限碳链异构)。
(2)等效氢法:
1、同一碳链上的氢等效;如:甲烷仅一种氢;
2、同一碳原子上所连甲基上的氢等效;
3、分子中处于对称位置上的氢等效。
书写同分异构体时,关键在于书写的有序性和规律性。
第一步,写出最长碳链:
第二步,去掉最长碳链中一个碳原子作为支链,余下碳原子作为主链,依次找出支链在主链中的可能位置(以下相似)
第三步,去掉最长碳链中的两个碳原子,作为两个支链(两个甲基):
1、分别连在两个不同碳原子上
2、分别连在同一个碳原子上
3、作为一个支链(乙基)
第四步,去掉最长碳链中的三个碳原子,
1、作为三个支链(三个甲基)
2、作为两个支链(一个甲基和一个乙基):不能产生新的同分异构体。
最后用氢原子补足碳原子的四个价键。
扩展资料
同分异构体的种类:
有机物产生同分异构体的本质在于原子的排列顺序不同,在中学阶段主要指下列三种情况:
(1)碳链异构:由于碳原子的连接次序不同而引起的异构现象,如CH3CH(CH3)CH3和CH3CH2CH2CH3。
(2)官能团位置异构:由于官能团的位置不同而引起的异构现象,如:CH3CH2CH=CH2和CH3CH=CHCH3。
(3)官能团异类异构:由于官能团的不同而引起的异构现象,主要有:
1、单烯烃与环烷烃:通式为CnH2n(n≥1)
2、二烯烃、单炔烃与环单烯烃:通式为CnH2n-2(n≥3)
3、苯及其同系物与多烯:通式为CnH2n-6(n≥6)
4、饱和一元醇与饱和一元醚:通式为CnH2nO(n≥2)
5、饱和一元醛、饱和一元酮、烯醇:通式为CnH2nO(n≥3)
6、饱和一元羧酸、饱和一元酯、羟基醛:通式为CnH2nO2(n≥2)
7、酚、芳香醇、芳香醚:通式为CnH2n-6O(n≥6)
8、葡萄糖与果糖;蔗糖与麦芽糖
9、氨基酸 [R-CH(NH2)-COOH]与硝基化合物(R’-NO2)
参考资料来源
百度百科-同分异构体
如何辨别有几种同分异构体
1,同位素是具有相同原子序数,中子数不同的原子如氕(氢)氘氚互为同位素。
2.核素是指具有一定数目质子和一定数目中子的一种原子。如C。Cu等
3.同素异形体是指是相同元素组成,不同形态的单质P 红磷白磷、
分子式为C4H8Cl2的同分异构体有多少种 麻烦画一下结构简式 高中化学
辨别有几种同分异构体有两种方法:
一、等效氢法
判断烃的一元取代物同分异构体的数目的关键在于找出“等效氢原子”的数目。“等效氢原子”是指:
1、同一碳原子上的氢原子是等效的。
2、同一碳原子所连甲基上的氢原子是等效的。
3、处于镜面对称位置上的氢原子是等效的。
二、书写方法
1、写出最长碳链
2、去掉最长碳链中一个碳原子作为支链,余下碳原子作为主链,找出支链在主链中的可能位置
3、去掉最长碳链中的两个碳原子,作为两个支链:连在两个不同碳原子上,连在同一个碳原子上,作为一个支链。
4、去掉最长碳链中的三个碳原子:作为三个支链,作为两个支链,不能产生新的同分异构体。
5、用氢原子补足碳原子的四个价键。
扩展资料:
应用:
同分异构现象广泛存在于有机物中,同分异构体的知识也贯穿于中学有机化学的始终。因此,分析、判断同分异构体也就成为有机化学的一大特点。
作为高考命题的热点之一,这类试题是考查学生空间想象能力和结构式书写能力的重要手段。考生在平时训练中就应逐渐领会其中的本质,把握其中的规律。
历史:
雷酸银和氰酸银是人类发现的第一个同分异构体。柏济力阿斯提出了一个崭新的化学概念,叫做“同分异性”。意思是说,同样的化学成分,可以组成性质不同的化合物。
氰酸与雷酸,便属于“同分异性”,它们的化学成分一样,却是性质不同的化合物。在此之前,化学界一向认为,一种化合物具有一种成分,绝没有两种不同化合物具有同一化学成分。
百度百科-同分异构体
同分异构体有九种,如图:
分子式为C4H8Cl2的有机物是饱和的卤代烃。如果主链为四个碳原子,从对称性上看,可以固定氯原子的位置有两个,将其固定在第一个碳原子上,可以有四种同分异构体:
1,1-二氯丁烷;1,2-二氯丁烷和1,3-二氯丁烷;1,4-二氯丁烷;将其固定在第二个碳原子上,有两种同分异构体,2,2-二氯丁烷;2,3-二氯丁烷。
如果主链为三个碳原子, 从对称性上看,可以固定氯原子的位置有两个, 将其固定在甲基碳原子上有3种:
即2-甲基-1,1-二氯丙烷;2-甲基-1,2-二氯丙烷;2-甲基-1,3-二氯丙烷;将其固定在非甲基碳原子上,出现的结构均与前面有重复,所以共计是9种。
扩展资料:
同分异构体的组成和分子量完全相同而分子的结构不同、物理性质和化学性质也不相同,
如乙醇和甲醚C2H6O。
同分异构体简称异构体。
有机物中的同分异构体分为构造异构和立体异构两大类。具有相同分子式,而分子中原子或基团连接的顺序不同的,称为构造异构。在分子中原子的结合顺序相同,而原子或原子团在空间的相对位置不同的,称为立体异构。
构造异构又分为(碳)链异构、位置异构和官能团异构(异类异构 )。立体异构又分为构象和构型异构,而构型异构还分为顺反异构和旋光异构(又称对映异构)。
百度百科-同分异构体









